药品包装密封完整性验证方法概述
目前,国内的一致性评价进行得如火如荼,其中CDE在一致性评价中多次提及注射剂密封性,并发布了“化学药品注射剂包装系统密封性研究技术指南”,本文针对多种密封性验证方法进行了阐述。
关键词:一致性评价,药品包装,注射剂,密封完整性,药典
版权所有:济南三泉中石实验仪器有限公司
国内外现有的药典中,涉及到密封完整性的有,美国药典USP1207 、欧洲EMA、中国CDE、国家药典委员会,其中以美国药典USP1207对容器密封完整性的概述较为完整:USP 1207.1包装完整性和测试方法的选择、USP 1207.2包装完整性泄漏测试方法、USP1207.3包装密封质量测试方法。欧洲EMA虽然强调容器密封性对于药品质量很关键,而且要进行相关的测试,但是并未发布针对性的容器密封性能研究指南。而CDE 发布了“化学药品注射剂包装系统密封性研究技术指南”,只是这个文件是个指导性文件。目前药典委已经委托国内相关的机构进行包装密封性的标准研究起草工作,济南三泉中石实验仪器有限公司有幸也参与到相关的起草工作,来完善国内的相关法规。因为尚未成型,我们不早做论述,只以较为完整的美国药典USP1207做一个概述。
目前美国药典USP1207将容器密封完整性的验证方法分为概率性方法和确定性测试方法。概率法,以微生物挑战法、染料穿透法(色水法)、气泡产生法在国内应用较为广泛。每种方法都对内容物和包装提出一些要求。
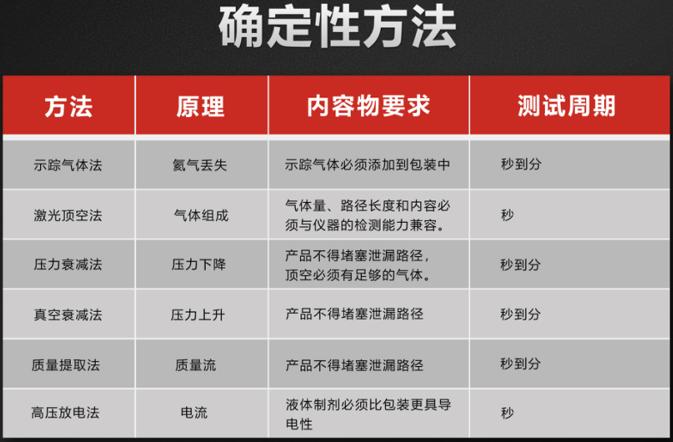
确定性方法是最近国内才逐步接受并广泛推广的测试方法,主要真空衰减法、压力衰减法、质量提取法、顶空气体法、高压放电法、示踪气体法等。随着国内技术的进步,确定性测试方法的相关测试技术已经与国际同类产品比肩,由于国产设备的价格优势,已经逐渐替代了价格高昂的进口设备。而由于确定性方法测试效率和测试精度较传统的概率法都有了较大提升,因此CDE“化学药品注射剂包装系统密封性研究技术指南”也提到“注射剂稳定性考察初期和末期进行无菌检查,其他时间点可采用包装系统密封性检查替代”。
由于无菌检查工作量极大,而且其破坏性使得样品的消耗量也很大,这也成为药品生产企业头痛的重点。如果稳定性考察时能解决这一问题,将大大降低药厂的人力物力成本。只是前期需要做好确定性方法的方法确认,及与微生物等方法的关联性能。尤其需要关注其灵敏度是否能够保证用户的最大可接受泄漏限度(MALL值)。同时,选择确定性方法时还要关注包装形式、包装材质、内容物、应用场景等众多因素,来选择适合药品本身特性的检测方法。
作为国内较早进行CCIT包装系统密封完整性检测技术研究的企业,已经帮助国内众多制剂企业通过了一致性评价。研发出的系列化产品,覆盖了多种方法,像真空衰减法(Leak-S微泄漏密封性测试仪)、压力衰减法(Leak-DS微泄漏密封性测试仪)、高压放电法(Leak-HV高压放电法密封性测试仪)。Sumspring三泉中石拥有专业团队,能够帮助药企完成药品包装密封完整性检查方法验证。
微泄漏密封性测试仪
目前,济南三泉中石实验仪器有限公司在概率法和确定性方法测试技术投入巨大研究力量,形成了系列化的密封性检测仪器,为国产仪器替代进口设备做出了应有的贡献。而且正在参与国家药典委员会组织的密封性测试方法的数据积累及验证工作。预计在不久的将来就会填补国内密封性测试标准这一空白。